L’absorption de la nicotine ŕ travers les membranes cellulaires
dépend du pH. En milieu acide, la nicotine est sous forme ionisée et ne passe pas
facilement les membranes. A pH physiologique (pH = 7.4), environ 31% de la
nicotine est sous forme non-ionisée et traverse aisément les membranes.
Le pH de la fumée de tabac est acide, cette acidité ne permet donc
qu’une faible absorption buccale. L’inhalation est donc nécessaire pour
permettre ŕ la nicotine d’ętre absorbée par l’énorme surface de l’épithélium
alvéolaire. Dans les poumons, la nicotine est rapidement absorbée par la
circulation systémique. Cette absorption est facilitée car le flux sanguin des
capillaires pulmonaires est élevé, représentant le passage de la totalité du
volume sanguin chaque minute. La nicotinémie augmente ainsi rapidement lors de
la consommation d’une cigarette. La nicotine absorbée se distribue rapidement
dans divers organes, et il ne lui faut qu’une dizaine de secondes pour
atteindre le cerveau (deux fois moins qu’aprčs une injection intraveineuse.)
La
forme active de la nicotine est un cation dont la charge se situe sur
l’azote du cycle pyrrole. Cette forme active ressemble ŕ l’acétylcholine
quant ŕ l’espace séparant les charges positives et négatives. L’acétylcholine
est une molécule flexible. Il existe deux types de récepteurs de l'acétylcholine: les récepteurs nicotiniques sur lesquels la nicotine peut se
fixer et les récepteurs muscariniques qui peuvent ętre activés par la
muscarine. La nicotine et la muscarine sont donc des agonistes spécifiques
d’un seul type de récepteurs cholinergiques (un agoniste est une molécule
qui se fixe sur le récepteur et mime l’effet du neurotransmetteur).
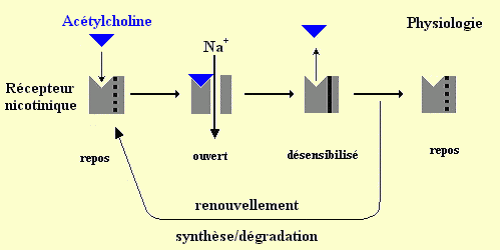
La nicotine a pour cible la neurotransmission cholinergique. Elle se fixe ŕ la place de l’acétylcholine sur les récepteurs nicotiniques cholinergiques, des récepteurs canaux. La liaison de l’agoniste sur le récepteur nicotinique provoque un changement de conformation de l’architecture protéique du récepteur, ce qui ouvre le canal ionique pendant quelques millisecondes. Le canal est sélectif pour les cations (surtout le sodium), son ouverture entraîne donc une brčve dépolarisation. Puis le canal se referme et le récepteur devient transitoirement réfractaire aux agonistes : c’est l’état de désensibilisation, qui est normalement suivi d’un retour ŕ l’état de repos, fermé et sensible aux agonistes. En cas d’exposition continue avec l’agoniste (męme ŕ faible dose), cet état de désensibilisation est durable (inactivation ŕ long terme.)
Cycle de fonctionnement d'un récepteur nicotinique :

Conditions normales physiologiques: aprčs ouverture
du canal sodique par liaison de l’acétylcholine, le récepteur passe par un
état désensibilisé avant de revenir au stade de repos ou d’ętre renouvelé.
[Figure reproduced courtesy of Dr. Sylvain Bartolami, INSERM U1198 "Mécanismes Moléculaires dans les Démences Neurodégénératives", Eq. 5 "Integrative Biology of Neuroregeneration", Université de Montpellier, France].
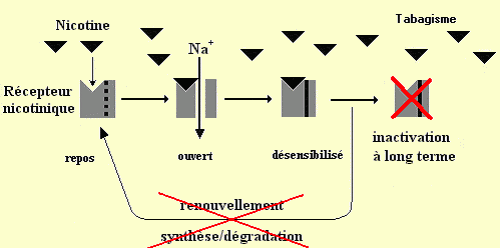
Conditions tabagiques: la nicotine remplace l’acétylcholine
et surstimule le récepteur nicotinique. Puis le récepteur est inactivé ŕ
long terme et son renouvellement est saturé par la nicotine.
[Figure reproduced courtesy of Dr. Sylvain Bartolami, INSERM U1198 "Mécanismes Moléculaires dans les Démences Neurodégénératives", Eq. 5 "Integrative Biology of Neuroregeneration", Université de Montpellier, France].
La nicotine élčve la stimulation des récepteurs cholinergiques nicotiniques. L’activation excessive et souvent chronique de ces récepteurs est compensée par une régulation ŕ la baisse du nombre de récepteurs fonctionnels. Cette réponse adaptative physiologique vise ŕ conserver l’homéostasie en maintenant la neurotransmission et la fonction cérébrale normales malgré une activation anormale des récepteurs. La réduction du nombre de récepteurs fonctionnels diminue l’effet psychotrope de la nicotine. C’est le phénomčne de tolérance qui incite le fumeur ŕ augmenter le nombre de cigarettes fumées afin d’obtenir un effet constant.
Par son action stimulante sur les récepteurs nicotiniques du systčme dopaminergique mésocorticolimbique (récepteurs présents sur les corps cellulaires des neurones de l’aire tegmentale ventrale et sur leurs terminaisons dans le noyau accumbens), la nicotine renforce la libération de dopamine dans le noyau accumbens. La dopamine est normalement libérée lors de comportements essentiels ŕ la survie de l’individu ou de l’espčce et produit de trčs fortes stimulations encéphaliques afin de faire éprouver du plaisir (c’est le circuit de récompense/renforcement.) Cependant, une exposition prolongée de ces récepteurs ŕ la nicotine réduit l’efficacité de cette derničre ; en effet, le fumeur maintient tout au long de la journée une concentration faible de nicotine dans son cerveau, cette faible concentration est suffisante pour maintenir une grande partie des récepteurs nicotiniques dans un état d’inactivation et pour ralentir leur renouvellement. L’autre facette du phénomčne d’inactivation est donc la baisse du plaisir ressenti.
Aprčs une brčve période d’abstinence (une nuit de sommeil par
exemple), la concentration cérébrale en nicotine diminue et
permet ŕ une partie des récepteurs de retrouver leur sensibilité. Le retour
de ces récepteurs ŕ un état fonctionnel hausse la neurotransmission
cholinergique ŕ un niveau anormal. Le fumeur éprouve donc de l’agitation et
de l’inconfort, ce qui l’incite ŕ fumer. Cette premičre cigarette de la
journée procure un plaisir maximum car la sensibilité des récepteurs
nicotiniques du systčme dopaminergique est maximale. Puis les récepteurs se désensibilisent
rapidement, la tolérance se développe et le plaisir diminue : c’est le
cercle vicieux du tabagisme.
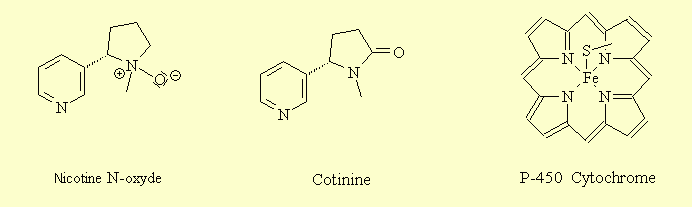
La nicotine est métabolisée principalement dans le foie, mais aussi un
peu au niveau des poumons et des reins. Les métabolites primaires de la
nicotine sont la cotinine et le N-oxyde de nicotine, produits de l’oxydation hépatique
de la nicotine par des cytochromes P-450.
En quoi est-ce que la nicotine peut s’avérer dangereuse pour
l’organisme ?
La nicotine et ses métabolites peuvent ętre trčs dangereux pour l’organisme. En effet, la nicotine constitue un puissant cancérigčne. En fait, en plus des réactions d’oxydation, la nicotine peut subir d’autres types de réactions métaboliques comme des réactions d’ouverture du cycle pyrrole qui correspond ŕ la partie non aromatique de la molécule. Il ne faut pas négliger la présence du groupement méthyle sur l’azote de ce cycle qui, s’il est détaché de la molécule, peut devenir un agent alkylant trčs puissant.
La fonction amine de la nicotine peut réagir avec du monoxyde d’azote, ou de l’acide nitreux, pour former une molécule de type « nitrosonium ». Ces derniers peuvent, comme la nicotine, ętre métabolisés, c’est-ŕ-dire oxydés et ouverts. Cette ouverture peut se faire de deux façons, et il se forme donc deux isomčres, deux molécules de type « nitrosamino » (R2N-N=O), oů l’un des groupements R est un méthyle. Cette réaction se produit de la façon suivante :
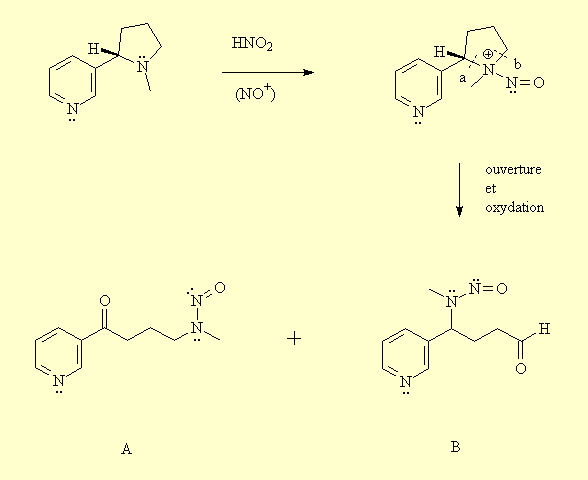
A
= 4 (N-méthyl-N-nitrosamino)-1-(3-pyridyl)-butan-1-one
B = 4 (N-méthyl-N-nitrosamino)-4-(3-pyridyl)-butanal
En présence d’acide, l’oxygčne du « nitrosamino »
est attaqué par un proton, ce qui engendre le déplacement de la liaison double
sur l’azote central, celui-ci devenant chargé positivement. La molécule
ainsi formée se comporte comme une source de méthyle. Le groupement « nitrosamino »
peut donc ętre attaqué par une autre amine, permettant ŕ l’azote de se libérer
de sa charge positive. Si l’amine attaquant le nitrosamino fait partie de la
structure d’une base azotée de l’ADN, il se produit alors une alkylation
irréversible de l’ADN :
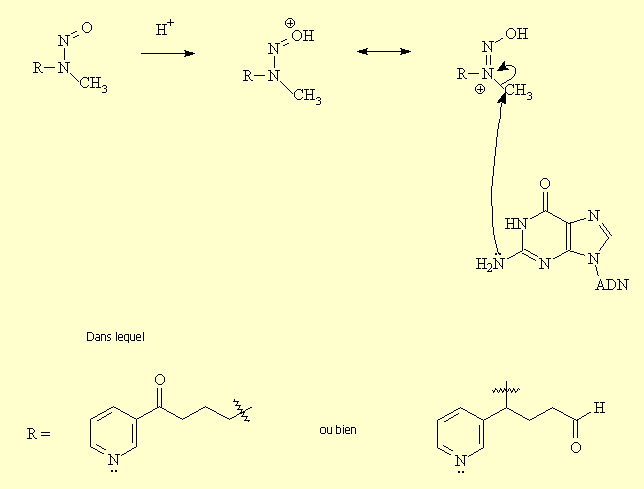
Cette alkylation est trčs nocive, et peut s’avérer cancérigčne puisqu’elle entrave le développement normal de la cellule. Si cette altération advient sur une partie de l’ADN impliquée dans la transcription d’un oncogčne, le développement d’une tumeur est assuré.